Tenacybakterioza należy do najpoważniejszych bakteryjnych chorób ryb morskich, a szczególnie dużym zagrożeniem stała się dla intensywnej hodowli łososia atlantyckiego w systemach morskiej akwakultury. Choroba ta, wywoływana przez bakterie z rodzaju Tenacibaculum, powoduje znaczne straty ekonomiczne poprzez zwiększoną śmiertelność obsad, obniżenie tempa wzrostu, pogorszenie jakości tuszy oraz rosnące koszty leczenia i profilaktyki. Zrozumienie biologii patogenu, czynników ryzyka, a także wdrożenie skutecznych strategii bioasekuracji i zarządzania zdrowiem stada ma kluczowe znaczenie dla zrównoważonej produkcji łososia i bezpieczeństwa łańcucha żywnościowego.
Charakterystyka tenacybakteriozy i jej znaczenie w hodowli łososia atlantyckiego
Tenacybakterioza jest chorobą bakteryjną wywoływaną głównie przez gatunki Tenacibaculum maritimum, T. dicentrarchi oraz kilka innych, słabiej poznanych przedstawicieli tego rodzaju. Są to bakterie Gram-ujemne, nitkowate, należące do rodziny Flavobacteriaceae, szeroko rozpowszechnione w środowisku morskim i przydennym. Patogeny te wykazują wysoką zdolność do kolonizacji skóry, płetw oraz skrzeli ryb, prowadząc do rozwoju zmian martwiczych i rozległych ubytków tkanek.
U łososia atlantyckiego tenacybakterioza występuje najczęściej po przeniesieniu narybku z wylęgarni słodkowodnych do klatek morskich, kiedy ryby przechodzą stres osmotyczny, transportowy i socjalny związany z zagęszczeniem obsad. Okres ten bywa krytyczny, ponieważ układ odpornościowy ryb jest silnie obciążony adaptacją do nowych warunków. Bakterie Tenacibaculum wykorzystują obniżoną odporność, uszkodzenia skóry i błon śluzowych, penetrują tkanki oraz wywołują przewlekłe lub ostre zakażenie.
Znaczenie tenacybakteriozy dla akwakultury łososia wynika z kilku nakładających się czynników. Po pierwsze, choroba obniża wydajność paszową – chore osobniki gorzej pobierają pokarm i przestają intensywnie rosnąć. Po drugie, uszkodzenia skóry i płetw prowadzą do obniżenia wartości handlowej tusz, co generuje straty na etapie przetwórstwa. Po trzecie, zwiększa się śmiertelność zarówno na początkowym, jak i późniejszych etapach tuczu, a leczenie wymaga stosowania antybiotyków lub szczepionek, co podnosi koszty produkcji. Wreszcie, obecność przewlekłych ognisk zakażenia w danym rejonie morskim wpływa na reputację producenta i może skutkować ograniczeniami handlowymi.
Szczególny problem stanowią koinfekcje – tenacybakterioza często występuje równolegle z innymi chorobami bakteryjnymi (np. wywołanymi przez Vibrio spp., Moritella viscosa) oraz pasożytniczymi, co komplikuje rozpoznanie i ogranicza skuteczność terapii. Ryby już osłabione np. przez inwazję pasożytów skórnych, takich jak wszy morskie, znacznie łatwiej ulegają zakażeniu Tenacibaculum, a przebieg kliniczny choroby jest cięższy i szybciej prowadzi do upadków.
Etiologia, patogeneza i obraz kliniczny tenacybakteriozy
Bakterie z rodzaju Tenacibaculum charakteryzują się zdolnością do tworzenia biofilmu, adhezji do powierzchni biologicznych oraz wytwarzania enzymów tkankowych, takich jak proteazy czy nukleazy, które degradują struktury komórkowe ryb. Pozwala im to nie tylko kolonizować powierzchnię ciała, ale też pogłębiać zmiany i penetrować w głąb tkanek. W sprzyjających warunkach środowiskowych (umiarkowana temperatura, podwyższony poziom substancji organicznej, wysokie zagęszczenie obsad) dochodzi do szybkiego wzrostu liczby bakterii w wodzie otaczającej klatki hodowlane.
Patogeneza zakażenia rozpoczyna się zwykle od kolonizacji skóry i płetw. Uszkodzenia mechaniczne, wynikające z ocierania się ryb o siatki, urządzenia, a także zadrapania powstałe podczas sortowania lub transportu, ułatwiają wnikanie bakterii. Ważnym czynnikiem jest także jakość wody – obecność cząstek stałych, uszkadzających nabłonek, a także zmiany zasolenia czy temperatury, obniżają szczelność bariery skórno-śluzowej. Błona śluzowa, stanowiąca pierwszą linię obrony immunologicznej, zostaje miejscowo przerwana, a Tenacibaculum może silnie przylegać do eksponowanej tkanki nabłonkowej.
Po przyczepieniu się do powierzchni komórek bakterie rozpoczynają wytwarzanie enzymów i toksyn, które prowadzą do martwicy miejscowej. Skutkiem jest powstawanie ognisk zapalnych, które rozwijają się w rozległe ubytki skóry o postępujących brzegach. Dochodzi także do niszczenia chrzęstnych i miękkich elementów promieni płetw, co skutkuje deformacjami i skróceniem płetw, a w zaawansowanych przypadkach niemal ich całkowitym zniszczeniem. Bakterie mogą również kolonizować skrzela, upośledzając wymianę gazową i prowadząc do niedotlenienia narządów wewnętrznych.
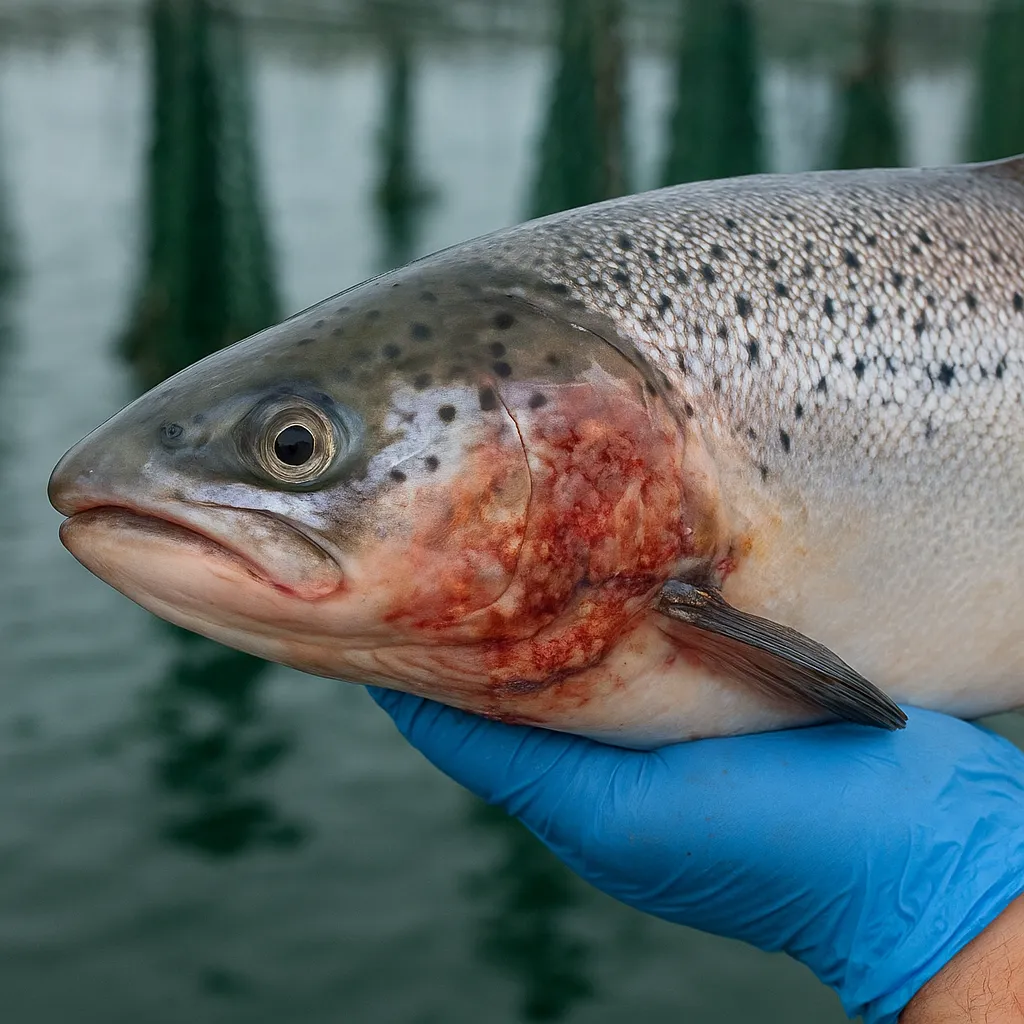
Obraz kliniczny tenacybakteriozy u łososia atlantyckiego jest dość charakterystyczny, choć w praktyce terenowej bywa mylony z innymi schorzeniami skóry i płetw. Do podstawowych objawów należy pojawienie się niewielkich ognisk owrzodzeń na powierzchni ciała, zwykle w okolicach głowy, pyska, nasady płetw oraz wzdłuż linii bocznej. Zmiany te przybierają postać szarawych, żółtawych lub czerwonawych plam pozbawionych łusek, z wyraźnie odgraniczonym, postrzępionym brzegiem. Z czasem ogniska te poszerzają się, łączą ze sobą, a w obrębie ubytku może dojść do odsłonięcia mięśni i tkanki podskórnej.
W przypadku ostrych zakażeń widoczna jest nasilona martwica płetw – promienie płetw ulegają nadżerkom, a płetwy zewnętrznie wydają się skrócone, z postrzępionymi krawędziami. Łuski wokół ognisk zapalnych często odstają, a powierzchnia ciała traci połysk. Ryby zachowują się apatycznie, utrzymują się bliżej powierzchni lub boków klatek, wykazują zmniejszoną aktywność żerową, a przy poważnym uszkodzeniu skrzeli dochodzi do szybkiego męczenia się przy pływaniu. Nasilone zakażenia mogą prowadzić do wtórnych infekcji innymi bakteriami oportunistycznymi, co znacznie pogarsza rokowanie.
Przebieg choroby bywa zróżnicowany – od łagodnych, przewlekłych zmian u niewielkiego odsetka obsady, po gwałtowne, ostre epizootie z wysoką śmiertelnością. Czynnikiem decydującym jest odporność ryb, gęstość obsady, stres środowiskowy oraz obecność innych patogenów. W stadach dobrze zarządzanych, z odpowiednią profilaktyką, tenacybakterioza może mieć formę endemicznego problemu, który wymaga stałego monitoringu, ale nie powoduje katastrofalnych strat. W warunkach zaniedbanej bioasekuracji choroba potrafi w krótkim czasie objąć większość obsady w danym gospodarstwie morskim.
Diagnostyka, bioasekuracja i strategie kontroli tenacybakteriozy
Skuteczne przeciwdziałanie tenacybakteriozie w morskiej akwakulturze wymaga wczesnego rozpoznania ognisk choroby oraz konsekwentnego wdrażania zasad bioasekuracji. Diagnostyka opiera się na połączeniu badań klinicznych, histopatologicznych oraz mikrobiologicznych. Pierwszym etapem jest rutynowa obserwacja stada – monitorowanie zachowania ryb, intensywności żerowania, wyglądu skóry i płetw. Przy podejrzeniu zakażenia pobiera się próbki tkanek ze zmian martwiczych, skrzeli oraz narządów wewnętrznych do badań laboratoryjnych.
W mikroskopii bezpośredniej stwierdza się obecność nitkowatych, Gram-ujemnych bakterii układających się często w charakterystyczne skupiska. Hodowla na selektywnych podłożach morskich oraz identyfikacja biochemiczna lub molekularna (PCR, sekwencjonowanie fragmentów genów) pozwala jednoznacznie potwierdzić przynależność do rodzaju Tenacibaculum i określić gatunek. Coraz częściej stosuje się także techniki biologii molekularnej do oceny stopnia zróżnicowania szczepów, ich zjadliwości i oporności na antybiotyki. Daje to możliwość śledzenia źródeł zakażeń i oceny skuteczności programów zwalczania choroby w skali regionalnej.
Kluczowym elementem strategii ograniczania tenacybakteriozy jest kompleksowa bioasekuracja, rozumiana jako zespół działań zapobiegających wprowadzaniu i rozprzestrzenianiu patogenów w gospodarstwie. Obejmuje ona zarówno zarządzanie ruchem ryb i sprzętu, jak i higienę wylęgarni, stacji smoltowych oraz farm morskich. Stosuje się ścisłą kontrolę pochodzenia materiału zarybieniowego, wymagając certyfikatów zdrowia i historii chorób w stadach macierzystych. Transport narybku odbywa się w zdezynfekowanych zbiornikach, z zastosowaniem środków minimalizujących stres, takich jak odpowiednia gęstość obsady, kontrola temperatury i natlenienia wody.
Na poziomie gospodarstwa morskiego zaleca się tworzenie stref o różnym statusie sanitarnym, ograniczanie przemieszczania personelu i sprzętu między klatkami oraz regularną dezynfekcję łodzi roboczych, siatek i narzędzi. Ważnym aspektem jest przeciwdziałanie mechanicznym uszkodzeniom skóry ryb – właściwe projektowanie i konserwacja klatek, unikanie ostrych krawędzi, racjonalne sortowanie i odłowy, wykonywane wyłącznie wtedy, gdy są niezbędne. Ograniczenie liczby manipulacji na rybach zmniejsza ryzyko uszkodzeń naskórka i otwiera mniej wrot zakażenia dla Tenacibaculum.
Duże znaczenie ma również zarządzanie parametrami środowiska wodnego w rejonie farm. W miarę możliwości kontroluje się obciążenie organiczne, by uniknąć nadmiernego zanieczyszczenia wody resztkami paszy i odchodami. Wysoka koncentracja materii organicznej stwarza dogodne warunki dla wzrostu bakterii i zwiększa ryzyko zakażenia. Dobór lokalizacji ferm morskich powinien uwzględniać prądy morskie, głębokość, temperaturę oraz wymianę wody, co pozwala ograniczyć kumulację patogenów w obrębie danej strefy produkcyjnej.
Farmy łososia atlantyckiego coraz częściej sięgają po środki immunoprofilaktyczne w postaci szczepień. Dostępne są szczepionki monowalentne i skojarzone, ukierunkowane na najważniejsze szczepy Tenacibaculum lub na kilka patogenów jednocześnie. Szczepienia przeprowadza się zazwyczaj na etapie smolta, jeszcze w środowisku słodkowodnym lub tuż przed transferem do morskich klatek. Ich skuteczność zależy od dokładnego dopasowania antygenów do lokalnie występujących szczepów oraz od stanu kondycyjnego ryb w momencie immunizacji. Odpowiednio opracowany program szczepień może znacząco ograniczyć częstość występowania klinicznej formy tenacybakteriozy i zmniejszyć liczbę ognisk choroby w kolejnych cyklach produkcyjnych.
W leczeniu aktywnych ognisk tenacybakteriozy stosuje się głównie chemioterapię, opartą na antybiotykach podawanych wraz z paszą. Wybór preparatu powinien być poprzedzony antybiogramem, gdyż w wielu rejonach świata obserwuje się narastającą oporność szczepów Tenacibaculum na najczęściej używane substancje czynne. Niewłaściwe, niemonitorowane stosowanie antybiotyków nie tylko zmniejsza skuteczność terapii, ale także stanowi zagrożenie dla środowiska morskiego i zdrowia publicznego. Dlatego coraz większą wagę przykłada się do ograniczenia chemioterapii na rzecz profilaktyki, szczepień oraz poprawy warunków hodowlanych.
Obok klasycznych metod kontroli chorób rozwijane są alternatywne strategie, obejmujące m.in. stosowanie probiotyków, prebiotyków, związków immunostymulujących oraz dodatków paszowych poprawiających integralność bariery jelitowej i skórno-śluzowej. Włączenie do paszy wybranych składników, takich jak β-glukany, nukleotydy czy wyciągi roślinne, może wspierać odporność nieswoistą ryb, co prowadzi do ograniczenia ciężkości przebiegu choroby po kontakcie z patogenem. Nie zastępują one środków bioasekuracji, ale stanowią cenne uzupełnienie strategii zarządzania zdrowiem stada.
W praktyce zarządzanie tenacybakteriozą wymaga ścisłej współpracy między producentami, lekarzami weterynarii ryb, laboratoriami diagnostycznymi oraz instytucjami nadzoru weterynaryjnego. Wspólne programy monitoringu zdrowia ryb, wymiana danych o występowaniu szczepów i ich właściwościach, a także koordynacja działań w obrębie całych regionów produkcyjnych (np. fiordów czy zatok) pozwalają ograniczyć ryzyko rozprzestrzeniania się choroby. Tworzone są regionalne plany zarządzania, określające rotację obsad, okresy przerw produkcyjnych oraz wymagania sanitarne przy zakładaniu nowych farm.
Tenacybakterioza w kontekście zrównoważonej akwakultury i przyszłych wyzwań
Rosnące zapotrzebowanie na białko pochodzenia zwierzęcego sprawia, że akwakultura, w tym hodowla łososia atlantyckiego, odgrywa coraz większą rolę w globalnej produkcji żywności. Jednocześnie intensyfikacja produkcji niesie ryzyko wzrostu presji chorób zakaźnych, a tenacybakterioza stała się jednym z typowych wyzwań dla rozwijających się ferm morskich. Utrzymanie równowagi między efektywnością ekonomiczną a bezpieczeństwem biologicznym i dobrostanem ryb wymaga inwestycji w nowoczesne technologie, badania naukowe i systemy zarządzania zdrowiem.
Jednym z istotnych kierunków rozwoju jest doskonalenie zamkniętych lub półzamkniętych systemów hodowlanych w środowisku morskim, takich jak klatki o ograniczonym kontakcie z wodą otwartą, systemy recyrkulacyjne wody morskiej czy obiekty offshore, oddalone od wybrzeży. Tego typu rozwiązania pozwalają lepiej kontrolować parametry środowiska, ograniczyć kontakt z dzikimi populacjami ryb, a tym samym zredukować poziom ekspozycji na środowiskowe szczepy Tenacibaculum. Jednocześnie wymagają one zaawansowanych metod monitoringu i automatyki, co podnosi próg wejścia dla mniejszych producentów.
Badania naukowe koncentrują się między innymi na poznaniu mechanizmów zjadliwości Tenacibaculum, strukturze ich genomu oraz odpowiedzi immunologicznej gospodarza. Dzięki sekwencjonowaniu całogenomowemu i analizom porównawczym możliwe jest identyfikowanie kluczowych czynników wirulencji oraz potencjalnych celów dla nowych szczepionek i terapii. Analiza relacji genotyp–fenotyp pozwala zrozumieć, dlaczego niektóre szczepy powodują ciężkie, szybko postępujące zmiany, podczas gdy inne wywołują jedynie łagodne uszkodzenia skóry lub bytują w środowisku w formie komensalnej.
Istotnym zagadnieniem jest rola mikrobiomu skóry i skrzeli ryb w zapobieganiu kolonizacji przez patogeny. Powierzchnia ciała łososia zasiedlona jest przez bogatą społeczność mikroorganizmów, które w warunkach równowagi działają jak naturalna bariera ochronna. Zaburzenia tego ekosystemu, wywołane stresem, nadmiernym stosowaniem środków dezynfekcyjnych czy antybiotyków, mogą otwierać drogę do zasiedlenia powierzchni ciała przez Tenacibaculum. Przyszłe strategie profilaktyczne prawdopodobnie będą w większym stopniu uwzględniały modulację mikrobiomu, np. poprzez probiotyki środowiskowe lub dodatki paszowe wpływające na skład flory bakteryjnej skóry.
Kolejnym obszarem badań jest poszukiwanie wskaźników wczesnego ostrzegania o zbliżającym się kryzysie zdrowotnym w stadzie. Rozwój narzędzi omicznych (transkryptomika, proteomika, metabolomika) umożliwia identyfikację zmian w organizmie ryby, które pojawiają się jeszcze przed wystąpieniem widocznych objawów klinicznych. Na podstawie paneli biomarkerów można potencjalnie przewidywać, kiedy stado wchodzi w stan podwyższonej wrażliwości na tenacybakteriozę, i odpowiednio wcześnie modyfikować zarządzanie, np. poprzez zmiany w żywieniu, ograniczenie zabiegów manipulacyjnych lub zwiększenie nadzoru weterynaryjnego.
W kontekście globalnych zmian klimatycznych pojawia się pytanie o wpływ ocieplenia wód morskich na epidemiologię tenacybakteriozy. Wzrost temperatury może sprzyjać szybszemu namnażaniu się bakterii, wydłużać sezon aktywności choroby i przesuwać jej zasięg geograficzny. Jednocześnie wyższa temperatura wody prowadzi do większego stresu fizjologicznego ryb, obniżając ich odporność i przyspieszając metabolizm. Konieczne jest zatem monitorowanie zmian klimatycznych w kontekście ryzyka chorób bakteryjnych oraz dostosowywanie praktyk hodowlanych do nowych warunków środowiskowych.
Nieodłączną częścią dyskusji o przyszłości morskiej akwakultury jest aspekt społeczny i regulacyjny. Rosnące oczekiwania konsumentów w zakresie bezpieczeństwa żywności, ograniczania stosowania antybiotyków i ochrony środowiska zmuszają producentów do poszukiwania bardziej zrównoważonych strategii radzenia sobie z chorobami, w tym z tenacybakteriozą. Tworzone są certyfikaty i standardy, które określają dopuszczalne praktyki w zakresie leczenia, profilaktyki i zarządzania gospodarstwem. Przestrzeganie tych standardów może być warunkiem dostępu do rynków zbytu o wysokiej wartości, co tworzy dodatkową motywację ekonomiczną do inwestowania w nowoczesne rozwiązania zdrowotne i bioasekuracyjne.
Warto zwrócić uwagę na rosnącą rolę edukacji i szkolenia personelu w gospodarstwach rybackich. Nawet najlepiej zaprojektowane procedury bioasekuracji nie przyniosą efektu, jeśli ich wdrażanie będzie niekonsekwentne lub nieprawidłowe. Każdy pracownik, od obsługi klatek po kadrę zarządzającą, powinien rozumieć podstawowe mechanizmy szerzenia się zakażeń, rozpoznawać pierwsze objawy choroby i znać procedury postępowania w sytuacji podejrzenia ogniska. Budowanie kultury bezpieczeństwa biologicznego jest procesem długotrwałym, ale stanowi fundament skutecznej obrony przed tenacybakteriozą i innymi chorobami zakaźnymi.
Ostatecznie tenacybakterioza w morskiej akwakulturze łososia atlantyckiego jest złożonym wyzwaniem, które wymaga połączenia wiedzy mikrobiologicznej, ekologicznej, weterynaryjnej i technologicznej. Tylko podejście systemowe, uwzględniające zarówno profilaktykę, diagnostykę, jak i odpowiedzialne leczenie, umożliwi długofalowe ograniczenie wpływu tej choroby na produkcję ryb, zachowanie dobrostanu zwierząt oraz ochronę środowiska morskiego.
FAQ – najczęściej zadawane pytania o tenacybakteriozę u łososia atlantyckiego
Jakie są najwcześniejsze objawy tenacybakteriozy u łososia atlantyckiego?
Najwcześniejsze objawy często są subtelne i łatwe do przeoczenia. Ryby mogą wykazywać lekką apatię, nieznaczny spadek żerowania oraz tendencję do przebywania bliżej powierzchni lub brzegów klatek. Na skórze pojawiają się drobne, odbarwione plamki pozbawione łusek, zwykle w okolicy głowy, pyska i nasady płetw. Z czasem zmiany te przybierają postać postrzępionych, powiększających się owrzodzeń, a płetwy stają się poszarpane i skrócone.
W jaki sposób dochodzi do zakażenia ryb bakteriami Tenacibaculum?
Zakażenie jest najczęściej następstwem kontaktu ryb z bakteriami obecnymi w wodzie morskiej lub na powierzchniach sprzętu i klatek. Patogeny wykorzystują mikrourazy skóry i płetw, powstałe w wyniku transportu, sortowania czy ocierania się o elementy konstrukcji, aby wniknąć w tkanki. Duże znaczenie ma też ogólny stan odporności – ryby zestresowane, przegęszczone i narażone na niekorzystne parametry środowiska znacznie łatwiej ulegają zakażeniu Tenacibaculum i rozwija się u nich pełnoobjawowa choroba.
Czy tenacybakterioza stanowi zagrożenie dla ludzi spożywających łososia?
Tenacybakterioza nie jest uznawana za klasyczną zoonozę, a przypadki zakażeń ludzi bakteriami Tenacibaculum są niezwykle rzadkie i dotyczą głównie osób z ciężkimi zaburzeniami odporności. W praktyce konsumenckiej ryzyko jest minimalne, ponieważ ryby przeznaczone do spożycia podlegają badaniom weterynaryjnym, a obróbka termiczna skutecznie eliminuje bakterie. Główne znaczenie choroby dotyczy zatem strat ekonomicznych w hodowli, a nie bezpośredniego zagrożenia dla zdrowia człowieka przy właściwym przygotowaniu produktu.
Jakie działania bioasekuracyjne są najskuteczniejsze w ograniczaniu choroby?
Największą skuteczność daje połączenie kilku elementów: kontrola pochodzenia narybku i jego zdrowotności, staranny transport przy minimalizowaniu stresu, dezynfekcja sprzętu i łodzi, ograniczanie ruchu między klatkami, a także właściwa konserwacja instalacji, by zmniejszyć uszkodzenia skóry ryb. Istotne jest też dostosowanie gęstości obsad do możliwości środowiska, regularny monitoring zdrowia stada oraz szkolenie personelu w zakresie rozpoznawania wczesnych objawów i zasad postępowania przy podejrzeniu ogniska tenacybakteriozy.
Czy istnieją skuteczne szczepionki przeciwko tenacybakteriozie u łososia?
W wielu krajach opracowano szczepionki przeciwko wybranym szczepom Tenacibaculum, często w formie preparatów skojarzonych obejmujących kilka ważnych bakteryjnych patogenów łososia. Ich skuteczność zależy od dopasowania antygenów do lokalnie krążących szczepów, jakości samego preparatu oraz momentu szczepienia względem okresu narażenia na zakażenie. Stosowanie szczepień nie eliminuje konieczności przestrzegania zasad bioasekuracji, ale może znacząco obniżyć częstość występowania ciężkich, klinicznych postaci choroby i ograniczyć użycie antybiotyków w cyklu produkcyjnym.













